گازهای آتشفشانی گازهایی هستند که از فعالیت های آتشفشانی ساطع می شوند . اینها شامل گازهای به دام افتاده در حفره ها (جیب ها) در سنگ های آتشفشانی ، گازهای محلول یا تفکیک شده در ماگما ، یا گازهایی است و گدازه که مستقیماً از گدازه یا به طور غیرمستقیم از طریق آب های زیرزمینی گرم شده در اثر فعالیت آتشفشانی ساطع می شوند .
منابع گازهای آتشفشانی روی زمین عبارتند از:
- مواد اصلی و بازیافتی از گوشته زمین ،
- اجزای جذب شده از پوسته زمین ،
- آب های زیرزمینی و جو زمین .
موادی که می توانند به گاز تبدیل شوند یا در اثر حرارت دادن گاز منتشر کنند، مواد فرار نامیده می شوند.
ترکیب
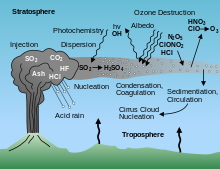
اجزای اصلی گازهای آتشفشانی عبارتند از بخار آب (H2O ) ، دی اکسید کربن (CO2 ) ، گوگرد به شکل سولفید دی اکسید (SO2 ) (گاز آتشفشانی با دمای بالا) یا سولفید هیدروژن ( H2S ) (کم). گازهای آتشفشانی درجه حرارت)، نیتروژن ، آرگون ، هلیوم ، نئون ، متان ، مونوکسید کربن و هیدروژن . سایر ترکیبات ، سولفید کشف شده در گازهای آتشفشانی عبارتند از: اکسیژن (شهاب سنگ)، کلرید هیدروژن ، هیدروژن فلوراید ، هیدروژن برومید ، اکسید نیتروژن (NOx ) ، هگزا فلوراید گوگرد کربونیل و ترکیبات آلی . ترکیبات ردیابی خارجی شامل جیوه ، هالوکربن ها (از جمله CFC و رادیکال های اکسید ) هالوژن هستند .
فراوانی گازها به طور قابل توجهی از آتشفشانی به آتشفشان دیگر، با آتشفشان و با محیط تکتونیکی متفاوت است. بخار آب همیشه فراوان ترین گاز آتشفشانی بوده است که اغلب بیش از 60 درصد از انتشار گازهای گلخانه ای را تشکیل می دهد. دی اکسید کربن معمولاً 10 تا 40 درصد از انتشار را تشکیل می دهد. [اولین]
آتشفشان هایی که در مرزهای صفحات همگرا قرار دارند ، بخار آب و کلر بیشتری نسبت به آتشفشان ها در نقاط داغ یا مرز صفحات واگرا منتشر می کنند . این به دلیل افزودن آب دریا به ماگمایی است که در مناطق فرورانش تشکیل می شود . آتشفشان های مرزی صفحه همگرا نیز نسبت های بالاتری از H 2 O / H 2 ، H 2 O / CO 2 ، CO 2 /He و N 2 /He در مقایسه با آتشفشان های واقع در نقاط داغ یا مرزهای شکاف دارند. [اولین]
ماگما و گازهای آتشفشانی با دمای بالا
ماگما حاوی اجزای فرار محلول است که در بالا توضیح داده شد. حلالیت این اجزا به فشار، دما و ترکیب ماگما بستگی دارد . با بالا رفتن ماگما به سطح، فشار محیط کاهش می یابد و حلالیت مواد فرار حل شده کاهش می یابد. هنگامی که حلالیت به زیر غلظت فرار میرسد، مواد فرار تمایل دارند از محلول موجود در ماگما خارج شوند (exsolve) و یک فاز گاز جداگانه (ماگمای فوق اشباع در مواد فرار) تشکیل میدهند.
گاز اولیه به صورت حباب های کوچکی در سراسر ماگما توزیع می شود که نمی توانند به سرعت از طریق ماگما بالا بروند. همانطور که ماگما بالا می رود، حباب ها از طریق ترکیبی از انبساط از طریق فشردگی و رشد ایجاد می شوند زیرا حلالیت مواد فرار در ماگما کاهش می یابد و باعث خروج گاز بیشتری می شود. بسته به ویسکوزیته ماگما، حباب ها ممکن است از طریق ماگما شروع به بیرون آمدن کرده و به هم بپیوندند، یا ممکن است نسبتاً در جای خود ثابت بمانند تا زمانی که شروع به اتصال کنند و شبکه ای از اتصالات را تشکیل دهند. در حالت اول، حبابها میتوانند از طریق ماگما بیرون بیایند و روی یک سطح عمودی، به عنوان مثال «سقف» یک اتاقک ماگما جمع شوند. در آتشفشان هایی که مسیر به سطح باز می شود، به عنوان مثال استرومبولی در ایتالیا ، حباب ها می توانند به سطح برسند و هنگامی که منفجر می شوند، انفجارهای کوچکی رخ می دهد. در حالت دوم، گاز می تواند به سرعت از طریق شبکه نفوذپذیر پیوسته به سمت سطح جریان یابد. این مکانیسم برای توضیح فعالیت در سانتیاگیتو، آتشفشان سانتا ماریا ، گواتمالا [2] و آتشفشان سوفریر هیلز استفاده شده است.
مونتسرات _ [3] اگر گاز نتواند به اندازه کافی سریع از ماگما فرار کند، ماگما را به ذرات خاکستر کوچک تقسیم می کند. خاکستر مایع نسبت به ماگمای چسبناک مقاومت بسیار کمتری در برابر حرکت دارد، بنابراین شتاب می گیرد و باعث انبساط بیشتر گاز و شتاب مخلوط می شود. این توالی وقایع باعث شد آتشفشان فوران کند. این که آیا گاز می تواند به آرامی فرار کند (فوران غیرفعال) یا نه (فوران انفجاری) توسط کل محتوای فرار ماگما اصلی و ویسکوزیته ماگما تعیین می شود که توسط ترکیب ماگما کنترل می شود .
اصطلاح گاز زدایی سیستم بسته به وضعیتی اطلاق می شود که گاز و ماگمای اصلی آن با هم معلق می شوند و در تعادل با یکدیگر هستند. ترکیب گاز ساطع شده در تعادل در فشار، دمایی که گاز از سیستم خارج می شود، با ترکیب ماگما است. در طی گاز زدایی سیستم باز، گاز از ماگمای اصلی خود خارج می شود و بدون حفظ تعادل با آن ماگما از طریق ماگمای بیش از حد بالا می رود. گاز خروجی سطح دارای ترکیبی است که میانگین ماگمای خروجی در اعماق مختلف است و معرف شرایط ماگمایی در هیچ عمقی نیست.
سنگ مذاب ( ماگما یا گدازه ) در نزدیکی جو گازهای آتشفشانی با دمای بالا (> 400 درجه سانتیگراد) را آزاد می کند. در طول فوران های آتشفشانی انفجاری، انتشار ناگهانی گاز از ماگما می تواند باعث حرکت سریع سنگ مذاب شود. هنگامی که ماگما با آب، آب دریا، آب دریاچه یا آب های زیرزمینی مواجه می شود، می تواند به سرعت تکه تکه شود. انبساط سریع گاز مکانیسم محرک اکثر فوران های آتشفشانی انفجاری است. با این حال، بخش قابل توجهی از انتشار گازهای آتشفشانی در طول مراحل شبه پیوسته آتشفشان فعال رخ می دهد.
گازهای آتشفشانی با دمای پایین و سیستم های هیدروترمال
هنگامی که گاز ماگمایی رو به بالا با آب شهابسنگ در آبخوان برخورد میکند ، بخار آب تولید میشود. گرمای نهان ماگما همچنین می تواند باعث بالا آمدن آب شهاب سنگ به صورت فاز بخار شود. فعل و انفعال طولانی مدت مایع و سنگ این مخلوط داغ می تواند اجزاء را از سنگ آذرین خنک کننده و سنگ کشور شسته و باعث تغییر حجم و انتقال فاز، واکنش و در نتیجه افزایش قدرت یونی یک مایع اسمزی رو به بالا شود. این فرآیند همچنین PH مایع را کاهش می دهد.
خنک کردن می تواند باعث جداسازی فاز و رسوب مواد معدنی شود که با تغییر بیشتر در شرایط احیا همراه است. ، در بیان سطحی چنین سیستم های گرمابی گازهای آتشفشانی با دمای پایین (کمتر از 400 درجه سانتیگراد) یا به صورت مخلوط گاز و بخار یا به صورت محلول در چشمه های آب گرم منتشر می شوند . در کف اقیانوس، چنین سیالات گرمابی فوق اشباع داغ، ساختارهای دودکش غول پیکری را تشکیل می دهند که به نام سیگارهای سیاه شناخته می شوند ، در نقطه انتشار به آب سرد دریا .
انتشار گازهای آتشفشانی غیر قابل انفجار
انتشار گاز می تواند با پیشروی از طریق ترک ها یا از طریق گاززدایی انتشاری در مناطق وسیعی از زمین نفوذپذیر مانند ساختارهای گاز زدایی منتشر (DDS) رخ دهد. در مکانهایی که از دست دادن گاز پیشرونده میشود، رسوب گوگرد و مواد معدنی کمیاب رسوبات گوگرد و دودکشهای کوچک گوگردی را تشکیل میدهد که به نام فومارول شناخته میشوند. ساختارهای فومارولیک در دمای بسیار پایین (زیر 100 درجه سانتیگراد) به نام سولفاتارا نیز شناخته می شوند. محل های گاز زدایی سرد عمدتاً دی اکسید کربن را موفت می نامند. چشمه های آب گرم آتشفشانی اغلب مقدار قابل اندازه گیری گاز ماگمایی را به صورت محلول نشان می دهند.
حسگرها، اکتساب ها و اندازه گیری ها
گازهای آتشفشانی از سال 1790 توسط Scipione Breislak در ایتالیا جمع آوری و تجزیه و تحلیل شده است. [4] ترکیب گازهای آتشفشانی به حرکت ماگما در داخل آتشفشان بستگی دارد. بنابراین، تغییرات ناگهانی در ترکیب گاز اغلب منادی تغییر در فعالیت آتشفشانی است. بر این اساس، بخش بزرگی از نظارت بر خطرات آتشفشانی شامل اندازهگیریهای معمول انتشار است. به عنوان مثال، افزایش محتوای CO2 در استرومبولی . به تزریق ماگمای غنی از فرار در عمق در سیستم نسبت داده شده است
گازهای آتشفشانی را می توان حس کرد (درجا اندازه گیری کرد) یا برای تجزیه و تحلیل بیشتر نمونه برداری کرد. حسگرهای گاز آتشفشانی می توانند:
- در گاز توسط حسگرهای الکتروشیمیایی و سلول های گازی طیف سنجی مادون قرمز
- خارج از گاز با استفاده از . طیفسنجی تلهمتری زمینی یا هوایی، برای مثال، طیفسنجی همبستگی (COSPEC)، طیفسنجی جذب نوری دیفرانسیل (DOAS) یا طیفسنجی فروسرخ تبدیل فوریه (FTIR)
سولفید دی اکسید (SO 2 ) در طول موج های فرابنفش به شدت جذب می شود و غلظت پس زمینه پایینی در جو دارد. این ویژگی ها دی اکسید سولفید را به یک هدف خوب برای نظارت بر گازهای آتشفشانی تبدیل می کند. می توان آن را با ابزارهای ماهواره ای که نظارت جهانی را امکان پذیر می کند و با ابزارهای زمینی مانند DOAS شناسایی کرد.
SO2 استفاده می شوند آرایه های DOAS در نزدیکی چندین آتشفشان با نظارت خوب قرار دارند و برای تخمین شار . سیستم تجزیه و تحلیل گاز چند جزئی (Multi-GAS) نیز برای CO2 و SO2 اندازه گیری از راه دور استفاده می شود. شار گازهای دیگر اغلب با اندازه گیری نسبت گازهای مختلف در جرم آتشفشان، به عنوان مثال FTIR، حسگرهای الکتروشیمیایی دهانه، یا نمونه برداری مستقیم و ضرب نسبت گاز، تخمین زده می شود .




نمونه برداری مستقیم گاز آتشفشانی
معمولاً با روشی انجام می شود که شامل یک فلاسک تخلیه شده با محلول سود سوزآور است که برای اولین بار توسط رابرت دبلیو بونسن (1811-1899) استفاده شد و سپس توسط شیمیدان آلمانی Werner F. Giggenbach (1937-1997) به نام خالص شد. گیگنباخ چای روشهای دیگر عبارتند از جمعآوری در ظروف خالی تخلیهشده، در لولههای شیشهای جریان، در بطریهای شستشوی گاز (اسکرابرهای سرد)، روی بستههای فیلتر آغشتهشده و روی لولههای جاذب جامد.
تکنیکهای تحلیلی برای نمونههای گازی شامل کروماتوگرافی گازی با تشخیص دمای رسانا (TCD)، تشخیص یونیزاسیون شعله (FID) و طیفسنجی جرمی (GC-MS) برای گازها، و سایر تکنیکهای شیمی مرطوب برای گونههای محلول (به عنوان مثال، تیتراسیون اسیدمتری برای محلولها). کروماتوگرافی CO و یونی برای سولفات ، کلرید ، فلوراید ). فلزات کمیاب، ایزوتوپها اجزای آلی و . اغلب با روشهای طیفسنجی جرمی مختلف تعیین میشوند
نظارت بر گازهای آتشفشانی
برخی از اجزای گازهای آتشفشانی می توانند نشانه های اولیه تغییر شرایط در عمق را نشان دهند و آنها را به ابزاری قدرتمند برای پیش بینی ناآرامی های قریب الوقوع تبدیل کند. در ارتباط با دادههای پایش لرزهای و تغییر شکل، پایش همبستگی بسیار مؤثر است. پایش گازهای آتشفشانی ابزار استاندارد هر رصدخانه آتشفشانی است . متأسفانه، دقیقترین دادههای مؤلفه هنوز به کمپینهای نمونهبرداری میدانی خطرناک نیاز دارند. با این حال، در دهه 1990 بسیار رشد کردهاند تکنیکهای سنجش از دور . پروژه کربنزدایی عمیق زمین از سنجش از راه دور Multi-GAS برای نظارت مستمر 9 آتشفشان استفاده میکند.
خطر
آتشفشانی مستقیماً مسئول حدود 3 درصد از مرگ و میرهای انسانی مرتبط با آتشفشان بین سالهای 1900 و 1986 هستند گازهای . دیگران بر اثر استنشاق دود جان خود را از دست دادند . گاز گلخانه ای ، دی اکسید کربن، که بی بو است، از آتشفشان ها ساطع می شود و تقریباً 1٪ از کل سالانه جهانی را تشکیل می دهد. [6] چندین گاز آتشفشانی از جمله سولفید دی اکسید، کلرید هیدروژن، سولفید هیدروژن، و هیدروژن فلوراید با دیگر ذرات اتمسفر واکنش داده و ذرات معلق در هوا را تشکیل می دهند . [اولین]